Решебник по химии за 10 класс (Г. Е.Рудзитис, Ф. Г.Фельдман, 2000 год), №1 к главе «Глава II. Предельные углеводороды (алканы или парафины) (стр. 22). Вопросы». Решебник по химии за 10 класс (Г. Е.Рудзитис, Ф. Г.Фельдман, 2000 год), №1 к главе «Глава II. Предельные углеводороды (алканы или парафины) (стр. 22). Вопросы».
|
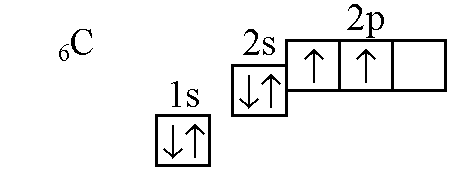
Условие задачи: №1. Как расположены электроны по энергетическим уровням и подуровням в атоме углерода? Почему в атоме углерода возможно распаривание 2s-электронов и какова у них форма электронных облаков?
Строение электронной оболочки атома углерода 1s22s22р2. У атома углерода четыре валентных электрона, из них только два неспаренных электрона на 2р-орбиталях.
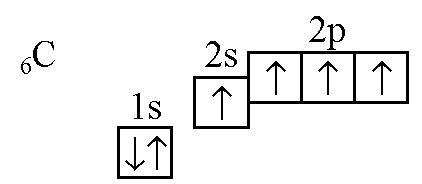
Однако на второй электронной оболочке есть еще свободная 2р-орбиталь, на которую может перейти один из электронов с 2s-орбитали. При этом у атома углерода становится четыре неспаренных электрона:
Таким образом, атом углерода может образовывать четыре ковалентные связи, причем происходит гибридизация орбиталей: образуются четыре абсолютно одинаковые орбитали, каждая из которых имеет форму вытянутой восьмерки, направленной к вершинам тетраэдра.