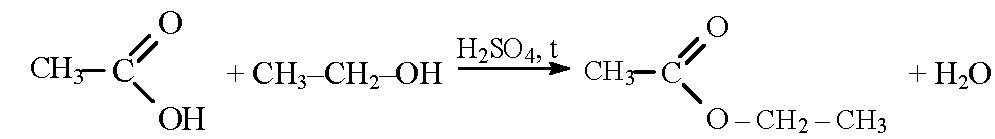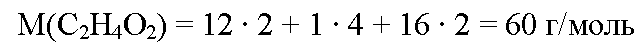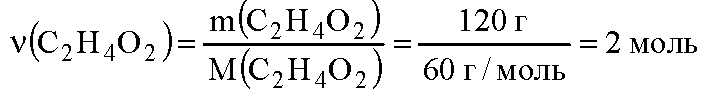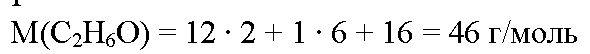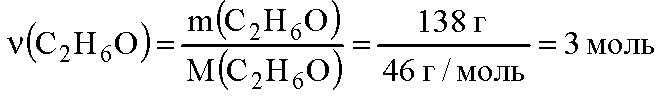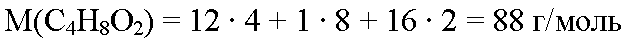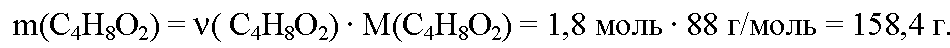Решебник по химии за 10 класс (Г. Е.Рудзитис, Ф. Г.Фельдман, 2000 год), №1 к главе «Глава IX. Сложные эфиры. Жиры. §§1, 2 (стр. 122) Задачи». Решебник по химии за 10 класс (Г. Е.Рудзитис, Ф. Г.Фельдман, 2000 год), №1 к главе «Глава IX. Сложные эфиры. Жиры. §§1, 2 (стр. 122) Задачи».
|
Условие задачи: №1. Сколько граммов этилацетата можно получить из 120 г уксусной кислоты и 138 г этанола, если выход сложного эфира составляет в массовых долях 0,9, или 90%, по сравнению с теоретическим?
Уравнение реакции:
Молекулярная формула уксусной кислоты С2Н4О2. Вычислим молярную массу уксусной кислоты:
Вычислим количество вещества уксусной кислоты:
Молекулярная формула этилового спирта С2Н6О. Вычислим молярную массу этилового спирта:
Вычислим количество вещества этилового спирта:
По уравнению реакции 1 моль уксусной кислоты реагирует с 1 моль этилового спирта, значит, для реакции с 2 моль уксусной кислоты необходимо 2 моль этилового спирта. Значит, этиловый спирт взят в избытке и расчет ведем по количеству вещества уксусной кислоты. По уравнению реакции из 1 моль уксусной кислоты образуется 1 моль этилацетата, значит из 2 моль кислоты при теоретическом 100% выходе получится 2 моль этилаце-тата. Однако реальный выход составляет 90%, или 0,9, следовательно получится 2 • 0,9 = 1,8 моль этилацетата.
Молекулярная формула этилацетата С4Н8О2. Вычислим молярную массу этилацетата:
Вычислим массу этилацетата: