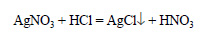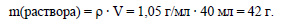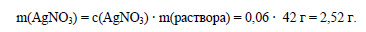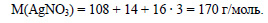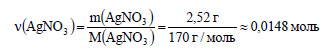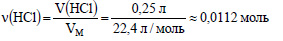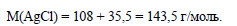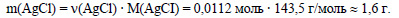Решебник по химии за 11 класс (Г. Е. Рудзитис, Ф. Г. Фельдман, 2000 год), №3 к главе «Глава VI. Неметаллы». Решебник по химии за 11 класс (Г. Е. Рудзитис, Ф. Г. Фельдман, 2000 год), №3 к главе «Глава VI. Неметаллы».
|
Условие задачи: В 40 мл 6%-го раствора нитрата серебра (1) (? = 1,05 г/см3) растворили 250 мл хлороводорода. Какое вещество и сколько по массе выпадает в осадок?
Решение:
Вычислим массу раствора нитрата серебра:
Вычислим массу нитрата серебра, содержащегося в растворе:
Определим молярную массу нитрата серебра:
Вычислим количество вещества нитрата серебра:
Вычислим количество вещества хлороводорода:
По уравнению реакции 1 моль хлороводорода реагирует с 1 моль нитрата серебра, значит для реакции с 0,0148 моль нитрата серебра необходимо 0,0148 хлороводорода, а имеется только 0,0112 моль, значит нитрат серебра взят в избытке, расчет ведем по хлороводороду. Из 1 моль хлороводорода образуется 1 моль хлорида серебра, значит из 0,0112 моль хлороводорода образуется 0,0112 моль хлорида серебра. Определим молярную массу хлорида серебра:
Вычислим массу хлороводорода:
Ответ: в осадок выпадает 1,6 г хлорида серебра.