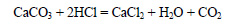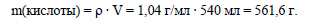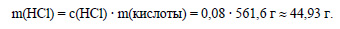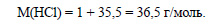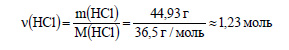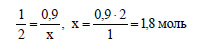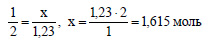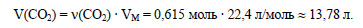Решебник по химии за 11 класс (Г. Е. Рудзитис, Ф. Г. Фельдман, 2000 год), №2 к главе «Глава VI. Неметаллы». Решебник по химии за 11 класс (Г. Е. Рудзитис, Ф. Г. Фельдман, 2000 год), №2 к главе «Глава VI. Неметаллы».
|
Условие задачи: На 0,9 моль карбоната кальция подействовали 540 мл 8%-ной соляной кислоты (? = 1,04 г/см3). Какой газ и сколько его по объему выделится?
Решение:
Выделяется оксид углерода (IV):
Вычислим массу соляной кислоты:
Вычислим массу хлороводорода, содержащегося в соляной кислоте:
Определим молярную массу хлороводорода:
Вычислим количество вещества хлороводорода:
По уравнению реакции 1 моль карбоната кальция реагирует с 2 моль хлороводорода. Пусть для реакции с 0,9 моль хлороводорода необходимо х моль хлороводорода. Составим пропорцию:
Необходимо 1,8 моль хлороводорода, а имеется только 1,23 моль. Значит, карбонат кальция взят в избытке, расчет ведем по соляной кислоте. По уравнению при взаимодействии 2 моль хлороводорода с карбонатом кальция выделяется 1 моль оксида углерода (IV). Пусть при взаимодействии 1,23 моль хлороводорода с карбонатом кальция выделяется х моль оксида углерода (IV). Составим пропорцию:
Вычислим объем оксида углерода (IV):
Ответ: выделится 13,78 л оксида углерода (IV).