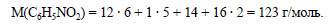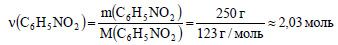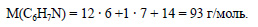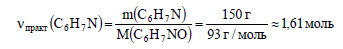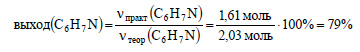Решебник по химии за 11 класс (Г. Е. Рудзитис, Ф. Г. Фельдман, 2000 год), №2 к главе «Глава XI. Амины. Аминокислоты. Азотсодержащие гетероциклические соединения». Решебник по химии за 11 класс (Г. Е. Рудзитис, Ф. Г. Фельдман, 2000 год), №2 к главе «Глава XI. Амины. Аминокислоты. Азотсодержащие гетероциклические соединения».
|
Условие задачи: При восстановлении 250 г нитробензола получили 150 г анилина. Вычислите, сколько это составляет процентов по сравнению с теоретическим выходом.
Решение:
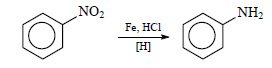
Уравнение реакции:
Молекулярная формула нитробензола С6Н5NO2. Вычислим молярную массу нитробензола:
Вычислим количество вещества нитробензола:
По уравнению реакции из 1 моль нитробензола получается 1 моль анилина, значит из 2,03 моль нитробензола при теоретическом 100%-ном выходе должно получиться 2,03 моль анилина. ?теор(С6Н7N) = 2,03 моль.
Молекулярная формула анилина С6Н7N. Вычислим молярную массу анилина:
Вычислим количество вещества практически полученного анилина:
Вычислим выход анилина:
Ответ: выход анилина равен 79%.