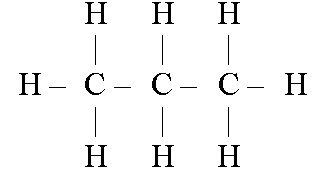Решебник по химии за 10 класс (Г. Е.Рудзитис, Ф. Г.Фельдман, 2000 год), №7 к главе «Глава I. Теория химического строения органических соединений. Электронная природа химических связей §§1-4 (стр. 11). Вопросы». Решебник по химии за 10 класс (Г. Е.Рудзитис, Ф. Г.Фельдман, 2000 год), №7 к главе «Глава I. Теория химического строения органических соединений. Электронная природа химических связей §§1-4 (стр. 11). Вопросы».
|
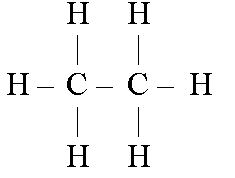
Условие задачи: №7. Какие противоречия выявились при определении валентности углерода: а) в молекуле этана С2Н6; б) в молекуле пропана С3Н6? Как эти противоречия устранила теория строения А. М. Бутлерова?
Если валентность водорода равна 1, то валентность углерода в молекуле
пропана должна быть равной 2⅔ , а валентность может быть равной только
целому числу. В этане валентность углерода равна 3, но обычно углерод четырехвалентен. Кроме того, этан и пропан во многом похожи по свойствам, следовательно, валентность углерода в них должна быть одинаковой.
Согласно теории Бутлерова, все атомы в молекуле связаны в определенной последовательности согласно их валентностям, причем валентность углерода всегда равна 4. Проблемы с определением валентности в молекулах
органических веществ вызваны тем, что в них есть связи между двумя атомами углерода:
этан
пропан