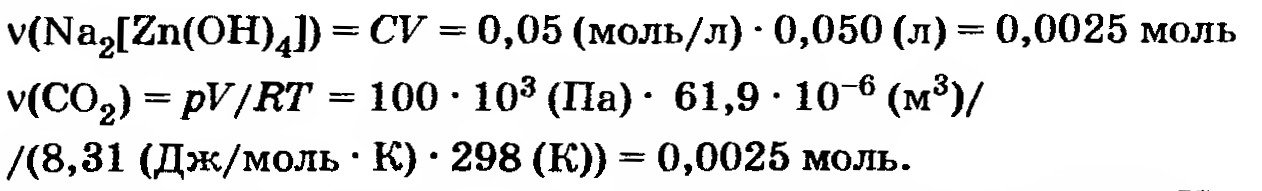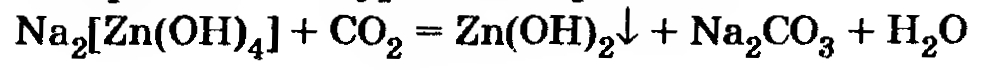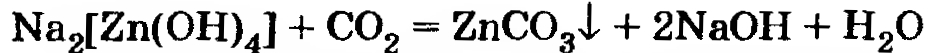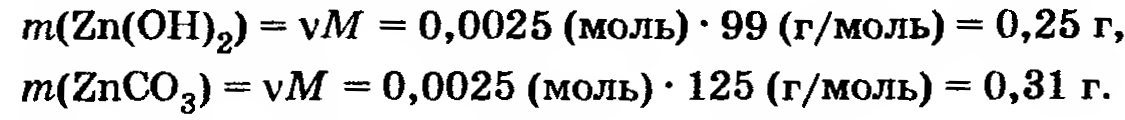 Решебник по химии за 10 класс (Л. С. Гузей, Р. П. Суровцева, 1999 год) , №7 к главе «Задачи к § 29.3». Решебник по химии за 10 класс (Л. С. Гузей, Р. П. Суровцева, 1999 год) , №7 к главе «Задачи к § 29.3».
|
Условие задачи: 7*. ММА96. Через 50 мл раствора Na2[Zn(OH)4] с концентрацией 0,05 моль/л пропустили 61,9 мл углекислого газа (100 кПа, 25 °С). Вычислите массу выпавшего осадка
В условии даны количества1 обоих реагентов. Следовательно, это задача на «избыток — недостаток». Начинать решение таких задач необходимо с определения количеств (в молях) каждого реагента.
1 Еще раз повторим, что слово «количество» в химии имеет два значения. Во-первых, это может быть количество вещества в общеупотребительном смысле — масса, объем, концентрация в растворе. Во-вторых, это может быть количество вещества как физикохимический термин, обозначающий число молей веществ». В данном тексте мы использовали сначала первое, а затем второе значение этого слова.
(Обратите внимание на перевод всех единиц в систему СИ.) Теперь запишем уравнение реакции:
или
В обоих случаях относительные количества реагентов (в молях) одинаковы. Без знания растворимости (без знания, какое вещество менее растворимо — именно оно должно образоваться) ответить однозначно нельзя. Поэтому целесообразно рассмотреть оба варианта. (На самом деле гидроксид цинка растворим несколько меньше, чем карбонат. Но это можно сказать, только обратившись к справочникам.)
Итак, количество вещества в осадке v = 0,0025 моль.