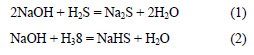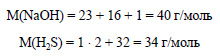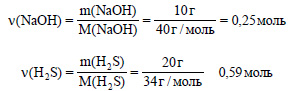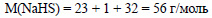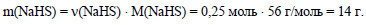Решебник по химии за 11 класс (Г. Е. Рудзитис, Ф. Г. Фельдман, 2000 год), №2 к главе «Глава II. Периодический закон и периодическая система Д. И. Менделеева на основе учения о строении атома». Решебник по химии за 11 класс (Г. Е. Рудзитис, Ф. Г. Фельдман, 2000 год), №2 к главе «Глава II. Периодический закон и периодическая система Д. И. Менделеева на основе учения о строении атома».
|
Условие задачи: Через раствор, содержащий 10 г гидроксида натрия, пропустили 20 г сероводорода. Какая соль образовалась при этом? Определите ее массу и количество.
Решение:
Возможно образование двух солей – сульфида натрия по уравнению (1) и гидросульфида натрия по уравнению (2).
Вычислим молярные массы гидроксида натрия и сероводорода:
Вычислим количество вещества гидроксида натрия и сероводорода:
По уравнению (2) 1 моль гидроксида натрия реагирует с 1 моль сероводорода, значит для реакции с 0,59 моль сероводорода нужно 0,59 моль гидроксида натрия, а по условию взяли только 0,25 моль. Следовательно, сероводород взят в избытке, и образуется гидросульфид натрия, расчет ведем по гидроксиду натрия. Из 1 моль гидроксида натрия по уравнению образуется 1 моль гидросульфида натрия, следовательно из 0,25 моль гидроксида натрия получится 0,25 моль гидросульфида натрия.
Вычислим молярную массу гидросульфида натрия:
Вычислим массу гидросульфида натрия:
Ответ: получится 0,25 моль (14 г) гидросульфида натрия.