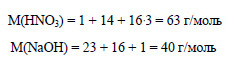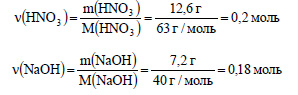Решебник по химии за 11 класс (Г. Е. Рудзитис, Ф. Г. Фельдман, 2000 год), №3 к главе «Глава III. Строение вещества». Решебник по химии за 11 класс (Г. Е. Рудзитис, Ф. Г. Фельдман, 2000 год), №3 к главе «Глава III. Строение вещества».
|
Условие задачи: К раствору, содержащему 12,6 г азотной кислоты, добавили раствор, содержащий 7,2 г гидроксида натрия. Сколько гидроксида по массе потребуется для полной нейтрализации?
НNО3 + NaOH =NaNО3 + Н2О
Вычислим молярную массу азотной кислоты и гидроксида натрия:
Вычислим количество вещества азотной кислоты и гидроксида натрия:
По уравнению реакции 1 моль азотной кислоты реагирует с 1 моль гидроксида натрия, следовательно 0,18 моль гидроксида натрия нейтрализуют 0,18 моль азотной кислоты. Всего же в растворе находится 0.2 моль азотной кислоты, то есть 0,2 – 0,18 = 0,02 моль азотной кислоты не прореагирует и для ее нейтрализации нужно дополнительно прибавить еще 0,02 моль гидроксида натрия.
Вычислим массу гидроксида натрия:
m(NaOH) = ?(NaOH) · M(NaOH) = 0,02 моль · 40 г/моль = 0,8 г.
Ответ: для полной нейтрализации кислоты нужно еще 0,8 г гидроксида натрия.