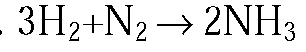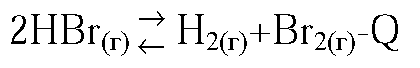Решебник по химии за 9 класс (А. М.Радецкий, 2011 год), №4 к главе «Тема II. Подгруппа кислорода. Основные закономерности течения химических реакций. Работа 2. Скорость химических реакций. Химическое равновесие.». Решебник по химии за 9 класс (А. М.Радецкий, 2011 год), №4 к главе «Тема II. Подгруппа кислорода. Основные закономерности течения химических реакций. Работа 2. Скорость химических реакций. Химическое равновесие.».
|
Условие задачи: Вариант 4
Вопросы:
1. Охарактеризуйте на конкретных примерах зависимость скорости химических реакций от катализаторов.
2. В какую сторону сместится равновесие реакции
2HBr(г) ↔ H2(г) + Br2(г) — Q а) при повышении температуры; б) при увеличении концентрации бромоводорода? Дайте обоснованный ответ.
Ответы и решения:
1
Без катализатора скорость этой реакции чрезвычайно мала, но при добавлении катализатора ее скорость значительно увеличивается.
2.
а) вправо, т. к. реакция эндотермична;
б) вправо, т. к. увеличивается концентрация исходного вещества.