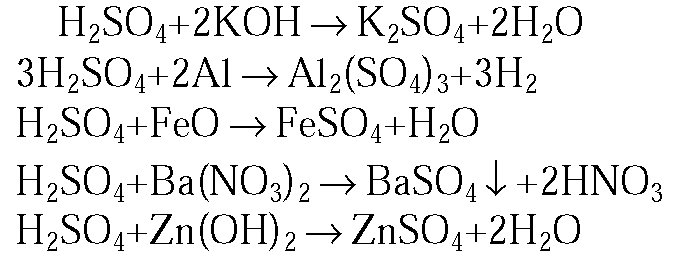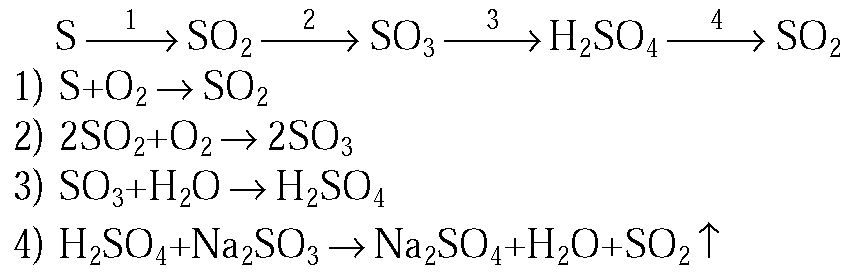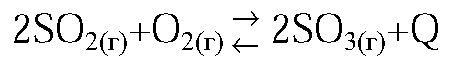Решебник по химии за 9 класс (А. М.Радецкий, 2011 год), №1 к главе «Тема II. Подгруппа кислорода. Основные закономерности течения химических реакций. Работа 3. Итоговая по теме II». Решебник по химии за 9 класс (А. М.Радецкий, 2011 год), №1 к главе «Тема II. Подгруппа кислорода. Основные закономерности течения химических реакций. Работа 3. Итоговая по теме II».
|
Условие задачи: Вариант 1
Вопросы:
1. С какими из перечисленных веществ будет реагировать раствор серной кислоты: гидроксид калия, алюминий, нитрат бария, оксид серы(IV), оксид железа(III), медь, гидроксид цинка? Напишите уравнения осуществимых реакций (два из них в ионной форме).
2. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
S →1→ SO2 →2→ SO3 →3→H2SO4
3. В какую сторону сместится равновесие реакции
2SO2(r) + O2(г) ↔ 2SO3(r) + Q а) при повышении температуры; б) при понижении давления? Дайте обоснованный ответ.
4. Рассчитайте массу озона, образующегося из 6 моль кислорода. {Ответ: 192 г.)
Ответы и решения:
1.
2.
3.
а) влево, т. к. реакция экзотермична;
б) влево, т. к. реакция протекает с уменьшением объема системы.
4. Увеличение скорости реакции обжига пирита достигается путем нагревания, постоянного тока кислорода, увеличения площади соприкосновения реагентов и катализатора.