Решебник по химии за 9 класс (Г. Е. Рудзитис, Ф. Г. Фельдман, 1999 год), №0 к главе «Лабораторные и практические работы». Решебник по химии за 9 класс (Г. Е. Рудзитис, Ф. Г. Фельдман, 1999 год), №0 к главе «Лабораторные и практические работы».
|
Условие задачи: Практическая работа № 3 стр. 74 Получение аммиака и опыты с ним. Ознакомление со свойствами водного раствора аммиака.
1) Получение аммиака и растворение его в воде
а) Действия: Насыпаем смесь
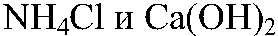
в пробирку. Закрываем газоотводной трубкой, конец которой направлен вверх. Нагреваем смесь. Наблюдения: Ощущается запах аммиака. Уравнения реакции:
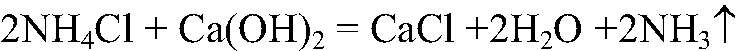
Выводы: Аммиак можно получить, нагревая смесь соли аммония и щелочи. б) Действия: Через некоторое время пробирку с аммиаком, не переворачивая, закрываем пробкой, затем опускаем в кристаллизатор с водой и открываем пробку. Наблюдения: Вода заполняет пробирку. Уравнения реакции:
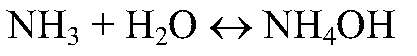
Выводы: Аммиак очень хорошо растворим, образует
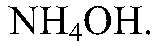
в) Действия: В полученный раствор помещаем красную лакмусовую бумажку. Добавляем к раствору фенолфталеин. Наблюдения: Бумажка синеет; раствор с фенолфталеином розовый. Уравнения реакции:
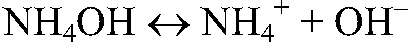
Выводы: Гидроксид аммония обладает основными кислотными свойствами.
2) Горение аммиака в кислороде
Действия: Нагреваем смесь
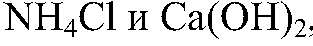
затем поджигаем с помощью лучинки газ, выходящий из газоотводной трубки. Наблюдения: Газ горит ярким пламенем. Уравнения реакции:
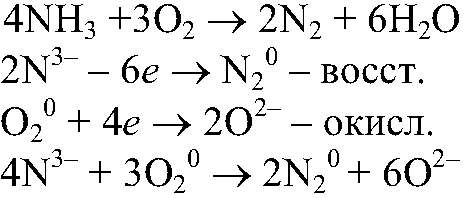
Выводы: В результате горения аммиака образуется азот и вода. Аммиак обладает восстановительными свойствами.
3) Взаимодействия аммиака с кислотами
Действия: Пробирку со смесью нагреваем. Газоотводную трубку последовательно вводим в пробирки с концентрированными кислотами
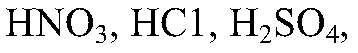
не касаясь поверхности кислот. Наблюдения: Появляется «белый дым». Уравнения реакции:
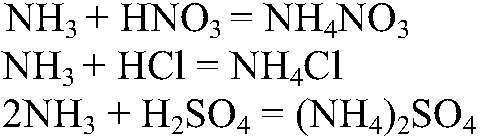
Выводы: Аммиак реагирует с кислотами, проявляя основ. св-ва.
4) Свойства водного раствора аммиака
а) Действия: Вводный раствор аммиака опускаем красную лакмусовую бумажку. Наблюдения: Бумажка синеет. Уравнения реакции:
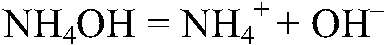
Выводы: Водный р-р аммиака обладает основными свойствами. б) Действия: К водному р-ру аммиака добавляем фенолфталеин Наблюдения: Раствор розовый. Уравнения реакции:
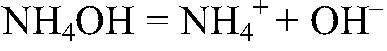
Выводы: В растворе аммиака присутствуют ионы
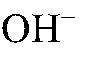
в) Действия: Добавляем разбавленную соляную кислоту. Наблюдения: Раствор обесцвечивается. Уравнения реакции: